
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
Gilteritinib fumarát
2023-12-02
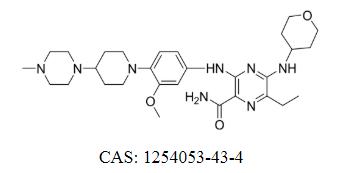
Gilteritinib fumarát Cas: 1254053-43-4
1. Pozadí
Cílené léky pro Gillette's (Gilteritinib) pro pacienty s akutní myeloidní leukémií žijí déle, lépe nedávno publikované v New England Journal of Medicine z výsledků velkých klinických studií ukazují, že: ve srovnání s chemoterapií použití cílených léků pro Gillette's (Gilteritinib, název komodity Xospata) může částečně zlepšit míru přežití pacientů s akutní myeloidní leukémií (AML).
Výsledky nového pokusu jsou povzbudivé. 371 pacientů zařazených do studie byli pacienti s AML se specifickou mutací genu FLT3, kteří byli dříve léčeni, ale později relabovali nebo nereagovali na léčbu (recidivující/refrakterní). Byli náhodně přiřazeni buď k léčbě Gilteritinibem, nebo ke standardní chemoterapii.
Výsledky ukázaly, že pacienti léčení pro léčbu přípravkem gillett, gilteritinib nejen žijí déle než pacienti podstupující chemoterapii (střední doba celkového přežití byla 9,3 měsíce až 5,6 měsíce) a je pravděpodobnější, že dosáhnou kompletní remise, počet bílých krvinek se vrátil na normální úroveň zcela nebo zčásti (pacienti léčení gilteritinibem (34 %), 15 %) u pacientů podstupujících chemoterapii.
2. Prezentace
Gilteritinib fumarát, vyvinutý společností Astellas, byl schválen Japonskou agenturou pro integrovanou farmaceutickou zdravotnickou zařízení a zařízení (PMDA) dne 21. září 2018, následně schválen americkým Úřadem pro kontrolu potravin a léčiv (FDA) dne 28. listopadu 2018 a Evropským úřadem pro léčiva (EMA) dne 24. října 2019 pod obchodním názvem Xospata®. Gilteritinib získal od FDA status rychlého a léku pro vzácná onemocnění.
Gilteritinib fumarát je inhibitor FLT3/AXL a přípravek Xospata® je schválen pro léčbu rekurentní nebo refrakterní akutní myeloidní leukémie s pozitivní mutací FLT3.
Xospata® je perorální tableta obsahující 40 mg gilteritinibu. Doporučená dávka je 120 mg jednou denně. Zvyšte nebo snižte dávku podle stavu pacienta, ale neměla by překročit 200 mg denně.
3. Cílové místo
AXL; FLT3
4. Mechanismus působení
inhibitory receptoru AXL; inhibitory FLT3
5. Indikace
Akutní myeloidní leukémie
6. Vývojová fáze
Schváleno k uvedení na trh dne 21. září 2018
7. R&D Company
Astellas
8. Cesta syntézy
8.1. Původní trasa
8.2. Naše trasa (optimalizovaná) – Lepší stabilita a vyšší výnos
8.3. Ros z KSM [CAS 2043020-03-5]
8.4. Stručný výrobní proces [CAS 2043020-03-5]
Krok 1:
K suspenzi NaOH byl přidán ethyl-3-oxopentanoát v jedné dávce a poté byla reakční směs míchána při teplotě místnosti. Byl přidán roztok NaN02 ve vodě a poté byla po kapkách přidána H2S04. Po kapkách byl přidán roztok NaOH a výsledná směs byla extrahována MTBE. Spojené organické vrstvy se promyjí solankou, suší se nad Na2S04, filtrují se a koncentrují se, čímž se získá produkt (E)-2-oxobutanaloxim.
Krok 2:
Suspenze (E)-2-oxobutanaloximu a aminomalononitril kyseliny p-toluensulfonové v IPA) se míchá při teplotě místnosti pod argonem. Po kontrole pomocí TLC byla reakční směs zfiltrována, koláč byl promyt IPA a vodou a vysušen, čímž byl získán 2-amino-3-kyano-5-ethylpyrazin-1-oxid.
Krok 3:
K suspenzi 2-amino-3-kyano-5-ethylpyrazin-1-oxidu v bezvodém DMF byl přidán POCI3 při 0 °C. Výsledná směs se míchá při 80 °C. Po kontrole pomocí TLC byla reakční směs pomalu přidána do směsi led/voda a extrahována MTBE. Spojené organické vrstvy se promyjí solankou, suší se nad Na2S04, filtrují se a koncentrují se, čímž se získá 3-amino-5-chlor-6-ethylpyrazin-2-karbonitril.
Krok 4:
K suspenzi t-BuONO a CuBr2 v DMF byl po kapkách přidán roztok 3-amino-5-chlor-6-ethylpyrazin-2-karbonitrilu v DMF. Po kontrole pomocí TLC byla reakční směs ochlazena na teplotu místnosti a poté nalita do směsi led/voda a extrahována MTBE. Spojené organické vrstvy se promyjí solankou, suší se nad Na2S04, filtrují se a koncentrují se, čímž se získá surový produkt, který se čistí chromatografií, čímž se získá 3-brom-5-chlor-6-ethylpyrazin-2-karbonitril.
9. Seznam meziproduktů, které můžeme dodat
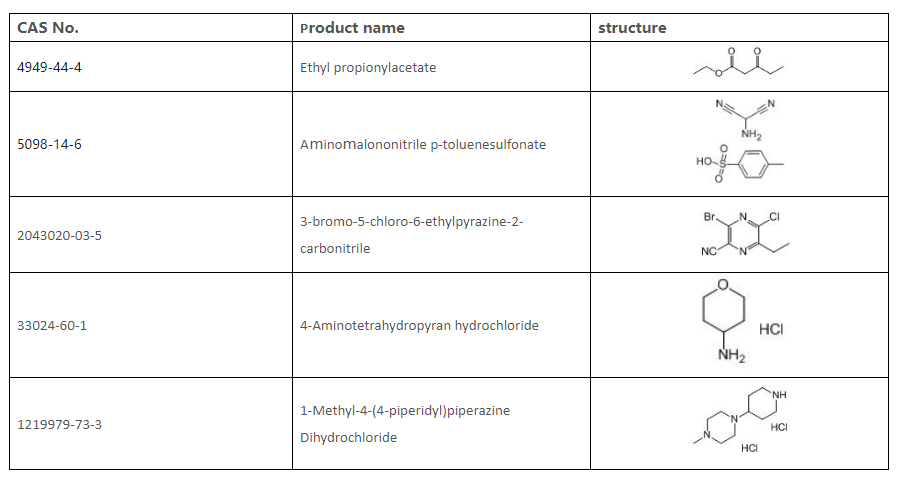
Sandoo Pharmaceutica je profesionální výrobce farmaceutických meziproduktů. Nabízíme kvalitní Gilteritinib Fumarate Cas: 1254053-43-4. Vítejte a těšíme se na váš dotaz!




